Bretziella fagacearum (précédemment nommé Ceratocystis fagacearum) (Flétrissement du chêne) - Fiche de renseignements
Identification
Nom : Bretziella fagacearum (Bretz) Z.W. de Beer, Marinc., T.A. Duong and M.J. Wingf (nouveau nom scientifique utilisé par l'ACIA depuis novembre 2018)
Synonyme : Chalara quercina Henry, Ceratocystis fagacearum (Bretz) Hunt
Forme imparfaite : Endoconidiophora fagacearum Bretz
Class. taxonomique : Fungi : Ascomycetes : Ophiostomatales
Noms usuels : Oak Wilt, Flétrissement du chêne
Carte de phytoravageur - Flétrissement du chêne
Principale maladie
Le flétrissement du chêne est dû au champignon Bretziella fagacearum qui se développe sur la partie externe de l'aubier. L'arbre infecté réagit en produisant des thylles et des gommes qui obstruent ensuite la circulation de la sève dans les tissus vasculaires atteints. L'arbre flétrit, puis meurt (French & Stienstra, 1980).
Éventail des hôtes
Toutes les espèces et variétés de chênes (Quercus spp.) testées se sont montrées sensibles au flétrissement, bien que certaines espèces du groupe des chênes rouges soient plus gravement affectées (French et Stienstra, 1980). Les essences de Quercus du groupe des chênes rouges meurent habituellement l'année durant laquelle l'infection s'est installée, alors que les chênes blancs se remettent de la maladie ou ne mourront de ses suites qu'après de nombreuses années.
Les essences suivantes sont considérées comme étant des hôtes (Farr et coll., 1989; Liese et Ruetze, 1987) :
- Quercus alba (chêne blanc)
- Quercus coccinea (chêne écarlate)
- Quercus ellipsoidalis (chêne Jack)
- Quercus falcata (chêne rouge, var. australe)
- Quercus fusiformis (chêne à feuilles fusiformes)
- Quercus ilicifolia (chêne à feuilles de houx)
- Quercus imbricaria (chêne alate)
- Quercus macrocarpa (chêne à gros fruits)
- Quercus marilandica (chêne des lieux arides)
- Quercus muehlenbergii (chêne jaune)
- Quercus nigra (chêne d'eau)
- Quercus rubra (chêne rouge)
- Quercus palustris (chêne des marais)
- Quercus phellos (chêne à feuilles de saule)
- Quercus prinus (chêne châtaignier)
- Quercus rubra (chêne rouge)
- Quercus rubra var. borealis (chêne rouge, var. boréale)
- Quercus stellata (chêne à lobes obtus)
- Quercus texana
- Quercus velutina (chêne noir)
- Quercus virgniana (chêne de Virginie)
Plusieurs variétés de pommiers (Malus) et de châtaigniers américains et européens (Castanea), ainsi que des espèces de chinquapins (Castanopsis) et de lithocarpes (Lithocarpus) se sont avérées sensibles à B. fagacearum à la suite d'une inoculation artificielle (Sinclair et coll., 1987; Rexrode et Brown, 1983).Bretz et Long (1950) ont signalé la découverte du champignon du flétrissement du chêne en milieu naturel, sur des châtaigniers chinois (Castanea mollissima), tardif que Rexrode et Brown (1983) ont souligné sa présence sur des arbres de plantation.
Répartition géographique
- Amérique du Nord : É.-U. (AL, IL, IN, IA, KS, KY, MD, MI, MN, MS, MO, NE, NC, OH, OK, PA, SC, SD,TN, TX, VA, WV, WI).
Biologie
Le flétrissement du chêne est une maladie vasculaire, c'est-à-dire que le champignon ne s'installe que dans les tissus vasculaires du xylème externe. Dans le cas des chênes rouges infectés, les spores peuvent se disséminer dans toutes les parties de l'arbre presque mourant, mais rarement dans les petites branches de moins de 3 à 4 pouces de diamètre (French et Stienstra, 1980). Bretziella fagacearum a été isolé dans le xylème des racines, du tronc, des branches, des ramilles et même des pétioles des feuilles chez les chênes rouges atteints (Gibbs et French, 1980). Chez les chênes blancs, le champignon se propage moins, se limitant au xylème de l'année. Si l'arbre se rétablit, le cerne de l'année enfouit l'infection sous le nouveau xylème, de sorte que les foyers précédents ne constituent pas une source majeure d'inoculum (French et Stienstra, 1980; Gibbs et French, 1980).
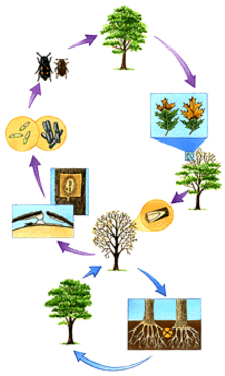
Propagation aérienne: Les Nitidulidés ou scolytes transportent les spores du champignon de la structure sporifère tapissante sur les arbres infectés à des lésions sur les arbres sains sur lesquels ils se nourrissent ou s'accouplent.
Propagation souterraine: Le champignon se propage dans le réseau de racines entrelacées d'arbres infectés et de sujets sains poussant à proximité les uns des autres.
Quand un chêne rouge infecté meurt, le champignon produit une structure sporifère tapissante dans l'écorce; à maturité, cette structure forme ensuite des conidies et des ascospores. Ces tapis sporifères sont de différentes dimensions, pouvant mesurer de 1-8 x 0,5-4 po à 13 x 7 po (French et Stienstra, 1980). Le champignon produit un grand nombre de conidies, mais les ascospores n'apparaissent qu'en présence de deux souches compatibles du champignon. Les structures sporifères ne se développent que sur les chênes rouges; elles n'apparaissent pas sur les chênes à feuilles fusiformes ni sur les chênes blancs (Davies, 1992). Elles se développent en général à la fin de l'automne ou au début du printemps et sont viables pendant deux à trois semaines seulement, attirant les insectes qui y circulent, s'y enfouissent et s'en nourrissent. Les spores gluantes adhèrent aux insectes qui les véhiculent ensuite jusqu'aux arbres sains où ils les déposent en pénétrant dans les lésions (Davies, 1992). On a observé la présence de structures sporifères surtout sur les troncs et les grosses branches, mais aussi sur des ramilles mesurant aussi peu que de 2 à 4 cm de diamètre (Gibbs et French, 1980). Dans la partie méridionale de l'aire de distribution du flétrissement du chêne, les structures sporifères tapissantes sont rares, la dissémination du champignon résultant surtout de l'activité des scolytes du chêne.
Bretziella fagacearum ne vit pas longtemps sur les arbres morts et disparaît habituellement des parties aériennes de l'hôte dans l'année qui suit la mort de l'arbre. Toutefois, il peut survivre beaucoup plus longtemps sur les parties souterraines.
À de nombreux endroits, le champignon se propage vers de nouveaux hôtes principalement par greffage naturel des racines entre arbres infectés et sujets sains. Dans certaines régions, tous les chênes poussant à proximité les uns des autres sont greffés ensemble, de sorte que la maladie se transmet très rapidement dans une telle colonie. La dissémination aérienne, moins courante, prend beaucoup plus de temps.
Vecteurs
Les scolytes du chêne Pseudopityophthorus minutissimus et P. pruinosus (Coléoptères, Scolytidés) sont considérés comme d'importants facteurs de propagation du flétrissement du chêne dans certaines régions. Dans la partie méridionale de l'aire de distribution de la maladie, les scolytes hivernent à tous les stades de leur développement, sauf sous celui de pupes, alors que dans le nord, seules les grosses larves survivent à l'hiver. Dans un cas comme dans l'autre, les scolytes adultes transportent les spores et, en se nourrissant, provoquent des lésions dans l'écorce à la bifurcation des ramilles, aux aisselles des feuilles, etc., créant ainsi des conditions propices au développement du flétrissement du chêne. On a noté que jusqu'à 30 p. 100 des scolytes émergeant de certains arbres étaient vecteurs du champignon, mais habituellement, ce taux varie entre 0,4 et 2,5 p. 100.
Les nitidules (Coléoptères, Nitidulidés) constituent apparemment un important groupe de vecteurs dans la partie septentrionale de l'aire de répartition du champignon. Au Minnesota, en Iowa, en Virginie-Occidentale et au Wisconsin, les nitidules propagent le champignon quand ils quittent les structures sporifères de B. fagacearum pour se diriger vers des blessures fraîches sur des arbres sains (Juzwik et coll., 1985). Les structures sporifères dégagent une odeur de fruit sucré qui attirent les insectes; quand ceux-ci circulent dessus, les spores gluantes adhèrent à leurs corps (French et Stienstra, 1980; Davies, 1992). L'effet combiné de la sporulation, de l'abondance des insectes vecteurs actifs et de la présence de lésions sur les arbres à la suite de l'émondage en mai et en juin rend cette période de l'année des plus propices à la dissémination de l'agent pathogène au Minnesota (Juzwik et coll., 1985).
Détection et identification
Symptômes
Dans le groupe des chênes rouges, les symptômes comprennent le flétrissement et le brunissement du feuillage commençant à la cime de l'arbre et aux extrémités des branches; ils se répandent ensuite rapidement à toute la couronne. Ces symptômes apparaissent d'abord en mai et persistent pendant toute la saison de croissance. Chaque feuille brunit progressivement, de l'extrémité à la base, laissant parfois une petite zone de tissu vert à la base, autour de la nervure médiane (French et Stienstra, 1980 - figure 3). Des feuilles à tous les stades de décoloration, y compris des feuilles vertes, tombent plus ou moins continuellement à mesure que la maladie s'aggrave. On peut aussi observer des taches diffuses dans la partie la plus externe de l'aubier, où le champignon a amené l'arbre à produire des gommes et des thylles qui entraînent la décoloration du bois (French et Stienstra, 1980).
Le champignon forme des endoconidies dans les structures sporifères grises ou chamois sous l'écorce des arbres infectés, mourants ou morts (figure 2). Sur certains arbres, le plus souvent des chênes rouges, les mycéliums à l'intérieur des structures sporifères s'agrandissent, constituant ainsi des coussinets qui exercent une pression suffisante pour soulever et fissurer l'écorce. Ce sont les masses sporifères qui dégagent l'odeur fruitée qui attirent les insectes. Le champignon s'attaque à des arbres de tous les âges, qui meurent habituellement la saison durant laquelle sont apparus les symptômes.
Les sujets du groupe des chênes blancs résistent mieux au flétrissement et peuvent vivre plusieurs années avant de mourir. Certains peuvent même se rétablir. Des chênes blancs peuvent être porteurs du champignon sans manifester de symptômes foliaires. En général, le brunissement est moins prononcé et la défoliation moins grave chez les chênes blancs, n'affectant souvent que quelques branches des sujets atteints. Les feuilles brunissent de l'extrémité vers la base et les profils de décoloration ressemblent au changement de couleurs des feuilles l'automne (French et Stienstra, 1980). On observe souvent des taches et des stries distinctives dans le xylème des branches infectées (figure 4), mais ce phénomène est moins fréquent chez les chênes rouges.
Les chênes à gros fruits affichent de leur côté une sensibilité intermédiaire entre celles des chênes rouges et des chênes blancs, car certains sont gravement affectés et meurent rapidement, alors que d'autres résistent longtemps, comme les chênes blancs (French et Stienstra, 1980).

Morphologie
Les échantillons de bois contenant du xylème sont cultivés sur de la gélose maltée forment des colonies grisâtres dégageant une odeur sucrée et fruitée. On peut aussi obtenir des cultures d'endoconidiophores et d'endospores. Des périthèces noirs apparaissent après 7 à 10 jours. Ils sont en forme de fioles et mesurent de 240 à 380 µm de diamètre et leur col dressé atteint de 250 à 450 µm de longueur. Les ascospores sont hyalines, unicellulaire et elliptiques; elles mesurent 2-3 X 5-10 µm et sont exsudées en une masse gluante blanc crème.
Dépistage et inspection
Les symptômes varient et ne sont pas toujours évidents, de sorte qu'il faut procéder à une analyse de laboratoire pour confirmer l'infection. Il faut prélever les échantillons de bois sur les branches (>2 cm de diamètre) ou les tiges principales, quand l'intérieur de l'écorce est encore frais et vert (OEPP, 2001). Plusieurs petits copeaux de bois, présentant chacun deux ou trois anneaux de croissance externes sont placés dans de la gélose maltée à 2 p. 100 après stérilisation dans de l'alcool suivie d'une incubation à la lumière ou dans l'obscurité pendant 8 à 10 jours à 20 à 25 °C avant l'examen.
Dans la culture, le mycélium se forme autour des copeaux après 3 à 5 jours. Les conidiophores apparaissent quant à eux en agrégats lâches souvent répartis irrégulièrement sur le mycélium. La culture est grise et dégage une odeur sucrée et fruitée. Le protocole de diagnostic de l'OEPP contient une description morphologique complète (OEPP, 2001). Les endoconidiophores et les endospores se forment et, si les deux types de structures de reproduction sont présentes, des périthèces exsudant les ascospores en une masse blanc crème apparaîtront aussi.
Mouvement et dispersion
La dissémination locale survient par greffage naturel des racines entre des arbres voisins ou à cause de la présence de divers insectes qui s'y alimentent et y creusent des galeries.
La propagation sur de grandes distances est prévisible à cause du commerce des produits du bois, en particulier du bois non écorcé qui pourrait abriter des scolytes du chêne, ou du matériel de pépinière infecté utilisé pour la plantation. Les structures sporifères peuvent se former sur jusqu'à 50 p. 100 des arbres infectés dans le groupe des chênes rouges, mais sont extrêmement rares chez les chênes blancs, de sorte que les premiers sont considérés comme constituant la voie la plus probable de transmission du flétrissement assistée par l'activité humaine (Liese et Ruetze, 1987). Le transport du bois de chauffage de chêne rouge peut aussi favoriser la dissémination du champignon, puisque les masses sporifères dans l'écorce attirent les insectes qui, à leur tour, véhiculeront les spores vers de nouvelles cibles (Davies, 1992). On croit que le bois de chauffage de chêne rouge est la principale source du flétrissement dans trois comtés de l'ouest du Texas, qui se trouvent à 150 milles ou plus du foyer principal (Davies, 1992). On peut isoler Bretziella fagacearum dans du bois d'oeuvre scié, et ce, jusqu'à 24 semaines après le sciage (Gibbs et French, 1980).
Rien ne prouve pour l'instant que les graines ou le feuillage des hôtes infectés contribuent à la propagation locale ou sur de grandes distances de Bretziella fagacearum.
Importance phytosanitaire
Impact économique et environnemental :
Dans le groupe des chênes rouges, les espèces de Quercus meurent habituellement l'année durant laquelle l'infection s'est installée, alors que les chênes blancs se remettent souvent de la maladie ou n'en meurent que de nombreuses années plus tard. La gravité de la maladie varie considérablement, mais l'infection est la plus sévère dans le nord-ouest de son aire de distribution (Gibbs et French, 1980). Bien que dans de nombreuses parties des zones infectées aux États-Unis l'impact soit minime sur l'économie locale fondée sur l'exploitation des forêts, au Texas, au Minnesota et dans le Wisconsin, on déplore la disparition rapide des chênaies, en particulier de celles constituées de Quercus fusiformis dans le sud et de Q. ellipsoidalis plus au nord.
Dans les zones urbaines où abondent les chênes sensibles, les répercussions sur la valeur des propriétés et sur d'autres valeurs sociales sont importantes. Ainsi, dans le centre du Texas, le flétrissement du chêne a provoqué un baisse draconienne de la valeur des propriétés tant en milieu urbain que rural à cause de la détérioration du paysage et de l'absence d'ombre. En 1990, le Texas Forest Service estimait les pertes à plus de 10 000 arbres, pour une valeur de plusieurs millions de dollars, dans la seule ville de Austin (Davies, 1992).
Lutte :
Il n'existe pas pour l'instant de remède pour les arbres atteints du flétrissement du chêne; la meilleure solution consiste donc à éviter ou à réduire l'infection dans les régions où sévit la maladie et à prévenir son introduction par inadvertance dans des zones actuellement indemnes (French et Stienstra, 1980).
Les mesures destinées à réduire le nombre de nouveaux foyers dans les régions déjà touchées incluent :
- la surveillance et l'enlèvement des arbres malades, ainsi que l'élimination des sources possibles d'inoculum;
- la prévention du greffage naturel possible des racines entre les arbres malades et les sujets sains et de l'aggravation de ce phénomène;
- la réduction au minimum des lésions causées aux arbres sains, notamment par émondage, en particulier pendant la période de vol des insectes vecteurs potentiels.
Comme toutes les espèces de chênes semblent le plus sensible aux infections dues aux spores disséminées par les insectes en mai et en juin, il importe d'éliminer toutes les sources d'inoculum susceptibles de produire des spores pendant cette période (French et Stienstra, 1980). Les chênes rouges malades sont les plus préoccupants comme sources futures d'infection, parce que B. fagacearum produit beaucoup plus de spores sur ce groupe d'arbres. Les chênes rouges qui flétrissent en juillet et en août peuvent donner lieu à la production de grandes quantités de spores le printemps de l'année suivante (French et Stienstra, 1980).
Il est possible de prévenir la propagation par greffage naturel des racines en creusant mécaniquement des tranchées autour des arbres ou des peuplements infectés au moyen d'équipement spécialisé ou de produits chimiques, comme le Vapam (méthyldithiocarbamate de sodium) ou un herbicide analogue qui tue les racines des arbres par contact (French et Stienstra, 1980).
Comme les arbres sains sont les plus sensibles à l'infection au printemps, il faut éviter de les émonder pendant cette période. De plus, les blessures dues à des bris lors de tempêtes ou à d'autres causes doivent être dûment traitées le plus rapidement possible (French et Stienstra, 1980).
Mesures phytosanitaires
Le traitement du bois et des grumes infectés à la vapeur ou par séchage au séchoir enraie Bretziella fagacearum (Gibbs et French, 1980). L'un ou l'autre des traitements suivants est efficace contre B. fagacearum infectant les grumes de chêne rouge (Quercus rubra, Q. velutina et Q. coccinea) :
- immersion complète des grumes dans de l'eau chaude à 49 °C ou plus pendant au moins 12 heures (Jones, 1973);
- immersion complète des grumes dans de l'eau chaude à 43 °C ou plus pendant au moins 48 heures (Jones, 1973);
- immersion complète des grumes dans de l'air chaud à 54 °C ou plus pendant au moins 24 heures (Jones, 1973);
- immersion complète des grumes dans de l'air chaud à 43 °C ou plus pendant au moins 48 heures (Jones, 1973).
La fumigation des grumes ou du bois d'oeuvre au bromure de méthyle est aussi une méthode d'éradication efficace du flétrissement du chêne; les taux suivants ont été appliqués avec succès en laboratoire et lors d'essais de fumigation au champ :
- grumes : 240 g/m3 de bromure de méthyle pendant 3 jours (72 heures) à des températures égales ou supérieures 5 °C (Schmidt et coll., 1982)
- grumes : 240 g/m3 de bromure de méthyle pendant 2 à 3 jours (48 - 72 heures) à des températures égales ou supérieures à 2 - 5 °C (MacDonald et coll., 1985)
- bois d'oeuvre : 240 g/m3 de bromure de méthyle pendant 2 jours (48 heures) à des températures égales ou supérieures à 5 °C (Schmidt, 1982).
La fumigation au bromure de méthyle à des températures inférieures à 0 °C est inefficace même si l'on augmente la concentration du fumigant et la durée du traitement (Schmidt, 1983). Le Treatment Manual Schedule T312 - PDF (5000 ko) (anglais seulement) du ministère américain de l'Agriculture (USDA) précise les taux autorisés pour l'éradication du flétrissement dans les grumes et le bois d'oeuvre de chêne.
Le fluorure de sulfuryle s'avère aussi efficace comme fumigant pour l'éradication de B. fagacearum dans les grumes de chêne, et offre une solution de rechange appropriée au bromure de méthyle quand on l'applique à des taux égaux ou supérieurs à 27 400 g h/m3 ou 280 g/m3 pendant 72 heures (Woodward et Schmidt, 1995; Schmidt et coll., 1997).
Les grumes de chêne rouge sont considérées comme étant un mode d'introduction beaucoup plus probable du flétrissement du chêne que celles de chêne blanc (Miller et coll., 1985). La pulvérisation d'une solution de nitrite de sodium à 10 p. 100 sur le bois parfait des grumes constitue un test de couleur simple permettant de distinguer le chêne rouge du chêne blanc et d'appliquer ainsi le traitement approprié au groupe. En effet, quand on pulvérise une telle solution sur le bois parfait de chêne blanc, la couleur change immédiatement. La zone pulvérisée tourne au jaune ou au brun légèrement orangé et, en cinq minutes, passe au brun foncé verdâtre ou pourpre à noir, avant de pâlir de nouveau dans les heures qui suivent (Miller et coll., 1985). Sur le bois de chêne rouge, le même traitement donne d'abord une première réaction analogue, soit une décoloration jaunâtre ou brune, mais le bois ne fonce pas par la suite.
Bibliographie
Bretz, T.W. and W.G. Long, 1950. Oak wilt fungus isolated from Chinese chestnuts. Plant Disease Reporter 34: 291.
Davies, C.S., 1992. Environmental Management of Oak Wilt Disease in Central Texas. Environmental Management 16: 323 - 333.
EPPO, 2001. Diagnostic protocols for regulated pests. Ceratocystis fagacearum. OEPP/EPPO Bulletin 31: 41 - 44.
Farr, D.F., G.F. Bills, G.P. Chamuris and A.Y. Rossman, 1989. Fungi on plants and plant products in the United States. APS Press, St. Paul, Minnesota, USA. 1252 pp.
French, D.W. and W.C. Stienstra, 1980. Oak Wilt. Extension Folder 310 - Revised 1980. Agricultural Extension Service, University of Minnesota. 6 pp.
Gibbs, J.N. and D.W. French, 1980. The transmission of oak wilt. USDA Forest Service Research Paper NC-185. 17 pp.
Jones, T.W., 1973. Killing the oak wilt fungus in logs. Forest Products Journal 23: 52 - 54.
Juzwik, J., D.W. French and J. Jeresek, 1985. Overland spread of the oak wilt fungus in Minnesota. J. Arboriculture 11: 323 - 327.
Liese, W. and M. Ruetze, 1987. On the risk of introducing oak wilt on white oak logs from North America. Arboriculture Journal 11: 237 - 244.
MacDonald, W.L., E.L. Schmidt and E.J. Harner, 1985. Methyl bromide eradication of the oak wilt fungus from red and white oak logs. Forest Products Journal 35: 11 - 16.
Miller, R.B., J.T. Quirk and D.J. Christensen, 1985. Identifying white oak logs with sodium nitrite. Forest Products Journal 35: 33 - 38.
Rexrode, C.O. and D. Brown, 1983. Oak Wilt. Forest Insect and Disease Leaflet 29. Northcentral Forest Experiment Station, Minnesota, USA. 5 pp.
Schmidt, E.L., 1982. Methyl bromide eradication of the oak wilt fungus from lumber. International Journal of Wood Preservation 2: 123 - 126.
Schmidt, E.L., 1983. Minimum temperatures for methyl bromide eradication of Ceratocystis fagacearum in red oak log pieces. Plant Disease 67: 1338 - 1339.
Schmidt, E.L., M.M. Ruetze and D.W. French, 1982. Methyl bromide treatment of oak wilt infected logs: laboratory and preliminary field fumigations. Forest Products Journal 32: 46 - 49.
Schmidt, E., J. Juzwik and B. Schneider, 1997. Sulfuryl fluoride fumigation of red oak logs eradicates the oak wilt fungus. Holz als Roh und Werkstoff 55: 315 - 318.
Sinclair, W.A., H.H. Lyon and W. T. Johnson, 1987. Diseases of trees and shrubs. Cornell University Press, Ithaca and London. 575 pp.
Wilson, A.D., 2001. Oak Wilt. A potential threat to southern and western oak forests. J. of Forestry 99: 4 - 11.
Text: Plant Health Risk Assessment Unit.
- Date de modification :

